Nuevo sistema de 10 colores con software Kaluza C que optimiza el flujo de trabajo y el informe de control de calidad para el análisis por citometría de flujo de leucemia y linfoma*
Miami, EE. UU. (24 de abril de 2019) - Beckman Coulter lanza el sistema ClearLLab 10C para laboratorios clínicos de citometría de flujo. El nuevo sistema es el primer panel de reactivos de inmunofenotipado para IVD de 10 colores aprobado por la Administración de Alimentos y Medicamentos (FDA) de los linajes linfoides y mieloides. Los cuatro tubos de anticuerpos secos premezclados utilizan la tecnología de la empresa DURA Innovations, que elimina la necesidad de pipetear anticuerpos y mejora la eficiencia junto con una menor posibilidad de errores humanos1, 2.
Junto con los paneles, el Sistema ClearLLab 10C integrado comprende
- Las células de control ClearLLab, una preparación líquida de eritrocitos y leucocitos humanos estabilizados (monocitos y granulocitos de linfocitos), son las primeras células de control para IVD de aplicación específica para el inmunofenotipado de L&L* como parte de un sistema validado.
- Las células de control ClearLLab incluyen valores de ensayo para los 27 marcadores actualmente disponibles en cuatro paneles ClearLLab10C, disponibles tanto para controles normales como anormales.
- Nuevas esferas de compensación ClearLLab para establecer compensación utilizando el kit de compensación ClearLLab, que incluye 10 tubos de color único para cada configuración de compensación.
- Software de análisis Kaluza C versión 1.1 o superior cuenta con funciones de control de calidad mejoradas en comparación con generaciones anteriores del software.
El sistema ClearLLab 10C incorpora el nuevo software Kaluza C de la empresa para agilizar y estandarizar la generación de informes clínicos de control de calidad según las directrices internacionales. Proporciona resultados de alta calidad a partir de combinaciones secas unificadas de marcadores de grupos de diferenciación (CD) utilizando la tecnología seca DURA Innovations de Beckman Coulter. Estas combinaciones de anticuerpos preformuladas ayudan al laboratorio a evitar posibles errores de preparación manual de cócteles de anticuerpos.
Los cuatro paneles ClearLLab 10C están diseñados específicamente para funcionar en los citómetros de flujo Navios y Navios EX de Beckman Coulter con un nuevo software de configuración de compensación avanzada. Al utilizar el sistema ClearLLab 10C, la compensación solo es necesaria en la configuración inicial de la aplicación, cuando el control de calidad diario falla, después de efectuar el servicio necesario del instrumento o al cambiar a un nuevo lote de Flow-Set Pro.
Con el sistema ClearLLab 10C, los laboratorios disponen ahora de una cartera de herramientas para inmunofenotipado que ayudan a proporcionar resultados precisos de pacientes para el análisis de L&L* en un entorno de laboratorio compatible, sin necesidad de efectuar exhaustivas tareas de validación, preparación y control de calidad manuales.
Recurso de formación exclusivo: Libro de casos ClearLLab 10C
ClearLLab 10C también es compatible con un recurso exclusivo, el Libro de casos ClearLLab 10C. El libro de casos proporciona 24 viñetas de diagnóstico que dan resultados característicos tras el análisis por citometría de flujo, con evaluación experta por hematopatólogos. Los laboratorios también pueden comparar la interpretación de sus propios hallazgos con el análisis en el libro de casos.
El Dr. Mario Koksch, vicepresidente y director general de la unidad de negocios de citometría de Beckman Coulter, afirmó: "El sistema ClearLLab 10C es una solución integrada que ofrece un flujo de trabajo estandarizado de laboratorio y mayor confianza en la consistencia y fiabilidad de sus hallazgos clínicos.
"Además, reduce los pasos de pipeteo, proclives a errores y de gran pérdida de tiempo, en pruebas desarrolladas en laboratorio, sustituyéndolos por una alternativa más eficiente en tiempo y que también simplifica la generación de informes clínicos de control de calidad."
Con el sistema ClearLLab 10C, el flujo de trabajo se reduce a cuatro pasos sencillos y estandarizados: procesamiento de muestras, adquisición de muestras, generación de informes y validación (consulte la Fig. 1).
Figura 1
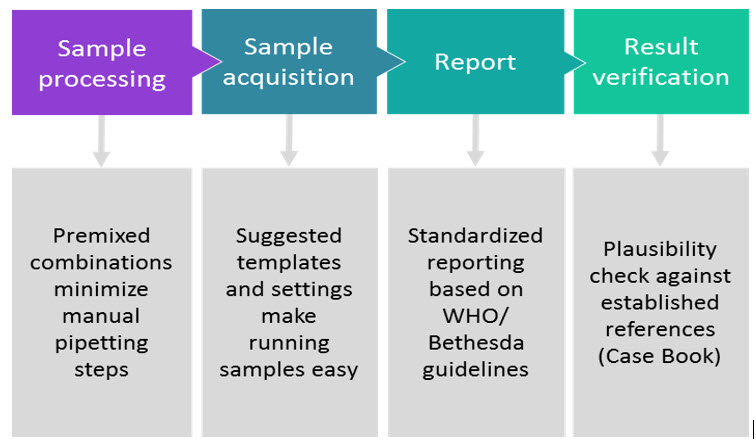
Los reactivos se pueden utilizar con sangre completa periférica (obtenida en K2EDTA, ácido-citrato-dextrosa [ACD] o heparina), médula ósea (obtenida en K2EDTA, ácido-citrato-dextrosa [ACD] o heparina) y muestras de ganglios linfáticos.
En 2017, los paneles de reactivos ClearLLab de cinco colores fueron los primeros cócteles de anticuerpos para IVD preformulados3 para el inmunofenotipado de leucemia y linfoma* con autorización de comercialización concedida a través del proceso De Novo de la FDA para uso en diagnóstico in vitro en EE. UU. Su autorización fue respaldada por un estudio del fabricante diseñado para demostrar el rendimiento de la prueba y que comparó los resultados de la prueba con los métodos de detección alternativos. La FDA indicó que ClearLLab proporcionó resultados coherentes como ayuda en los diagnósticos de estos cánceres graves.
Los reactivos ClearLLab siguen las recomendaciones de consenso internacional de Bethesda 2006 sobre el análisis inmunofenotípico por citometría de flujo de la neoplasia hematolinfoide4. Son compatibles con la clasificación revisada en 2016 de la Organización Mundial de la Salud (OMS) de neoplasias mieloides y leucemia aguda. La OMS, en colaboración con la Asociación Europea de Hematología y la Sociedad de Hematología, ha realizado recientemente importantes cambios en la clasificación de estas enfermedades. Estas incluyeron nuevos criterios para el reconocimiento de algunas neoplasias descritas previamente, así como la aclaración y el perfeccionamiento de los criterios definitivos para otras5.
*En el caso de linfoma, se refiere únicamente al linfoma no Hodgkin
Referencias
- Rajab A, Axler O, Leung J, Wozniak M, Porwit A. Ten- color 15-antibody flow cytometry panel for immunophenotyping of lymphocyte population. International Journal of Laboratory Hematology 2017 May;39 Suppl 1:76-85. doi: 10.1111/ijlh.12678.
- Smallwood C, Galama L, Apoll L, Heinrich KH, Demers J, Buchanan S. Examining the economic impact of laboratory defined testing a flow cytometry immunophenotyping for hematologic malignancies: an analysis of heath resource utilization. Sesión de póster presentada en: Sociedad internacional de farmacoeconomíaa e investigación de resultados (ISPOR), 18.º Congreso Europeo Anual, Milán, Italia. 09 al 13 de noviembre de 2015
- Administración de Alimentos y Medicamentos de los Estados Unidos, anuncio de prensa, 29 de junio de 2017: https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm565321.htm
- Davis BH, et al. 2006 Bethesda International Consensus Recommendations on the Immunophenotypic Analysis of Hematolymphoid Neoplasia by Flow Cytometry: Optimal Reagents and Reporting for the Flow Cytometric Diagnosis of Hematopoietic Neoplasia. Cytometry Part B (Clinical Cytometry 2007 72B: S5-S13
- Vardiman JW, Arber DA, Brunning DR et al. The 2008 revision of the World Health Organization (WHO) classification of myeloid neoplasms and acute leukemia: rationale and important changes. Blood 2009 114:937-951; doi: 10.1182/blood-2009-03-209262.

